Das Delir oder Delirium ist eine akute organisch verursachte Psychose und bezeichnet ein ätiologisch unspezifisches Syndrom, charakterisiert durch Störungen des Bewusstseins mit akutem Beginn und undulierendem Verlauf, mit speziellem Augenmerk auf die qualitative Bewusstseinsstörung im Sinne von Aufmerksamkeitsstörung und Verwirrtheit. Veränderungen der kognitiven Funktionen, der Wahrnehmung, der Psychomotorik sowie Störungen des Schlaf-Wach-Rhythmus sind weitere Symptome. Die Infobox beschreibt die diagnostischen Kriterien des Delirs nach dem ICD-10 (International Classification of Diseases, 10th revision).
Bei der Kodierung des Delirs unterscheidet man zwischen dem Delir ohne Demenz (ICD-10: F05.0) oder bei Demenz (F05.1), dem Delir mit gemischter Ätiologie (zum Beispiel das postoperative Delir, F05.8) sowie dem Delir „nicht näher bezeichnet“ (F05.9). In der Fachliteratur geht man davon aus, dass geschätzte 30 bis 60 Prozent der Delirien im stationären Setting unerkannt bleiben, vor allem das in weiterer Folge beschriebene hypomotorische Delir (hypokinetisches Delir, „stilles Delir“, akute Verwirrung ohne Agitation) wird oft übersehen. Fallweise wird statt dem Delir eine Depression oder eine Demenz diagnostiziert, wobei demente Patienten tatsächlich besonders anfällig für ein Delir während der Krankenhausaufenthalte sind (Erkinjuntti et al., 1986). Ein Delirium vergrößert die Mortalität bei und nach stationären Aufenthalten signifikant (McCusker et al., 2002), die richtige und frühe Diagnosestellung sowie adäquate Therapien verbessern die Prognose jedoch deutlich.
Das Erkennen einer Komorbidität von Demenz und Delir ist somit auch von wesentlicher klinischer Bedeutung, wie im Konsensus-Statement der Österreichischen Gesellschaft für Neuropsychopharmakologie und Biologische Psychiatrie (ÖGPB) erläutert wird (Kasper et al., 2015). Ein Delir ist die häufigste Komplikation beim hospitalisierten, über 65-jährigen Patienten und tritt in dieser Altersgruppe bei etwa 15 Prozent aller Patienten an internistischen Abteilungen (Erkinjuntti et al., 1986) und bei 30 bis 40 Prozent der Patienten an chirurgischen Abteilungen auf. Relativ viel Literatur gibt es zum postoperativen Delir im Kontext mit orthopädischen und kardialen Eingriffen bei älteren Menschen. Beinahe 40 Prozent aller Patienten nach einer Operation wegen Hüftfraktur zeigen Symptome eines Delirs. Eine hohe Inzidenz zeigt sich auch bei Patienten nach herzchirurgischen Operationen. Im postoperativen, intensivmedizinischen Kontext wird oft der Begriff „Durchgangssyndrom“ synonym für das Delir verwendet, weil ein Abklingen der postoperativen Verwirrtheit postuliert wird.
Infobox
Das Delir im ICD-10 (International Classification of Diseases, 10th revision):
- Bewusstseinsstörung mit verminderter Aufmerksamkeit oder Unfähigkeit, diese zuzuwenden, zu richten, zu halten
- Globale Störung der Kognition, Verwirrtheit, Merkschwäche, Wahrnehmungsstörungen (mit Verkennungen, optischen Halluzinationen), Wahnphänomenen
- Psychomotorische Störungen
- hypermotorische oder hypomotorische Delirien
- Störung des Schlaf-Wach-Rhythmus
- Akuter Beginn und Schwankungen
Eine kausale zerebrale oder systemische Erkrankung wird vermutet.
1. Die Behandlung des Delirs
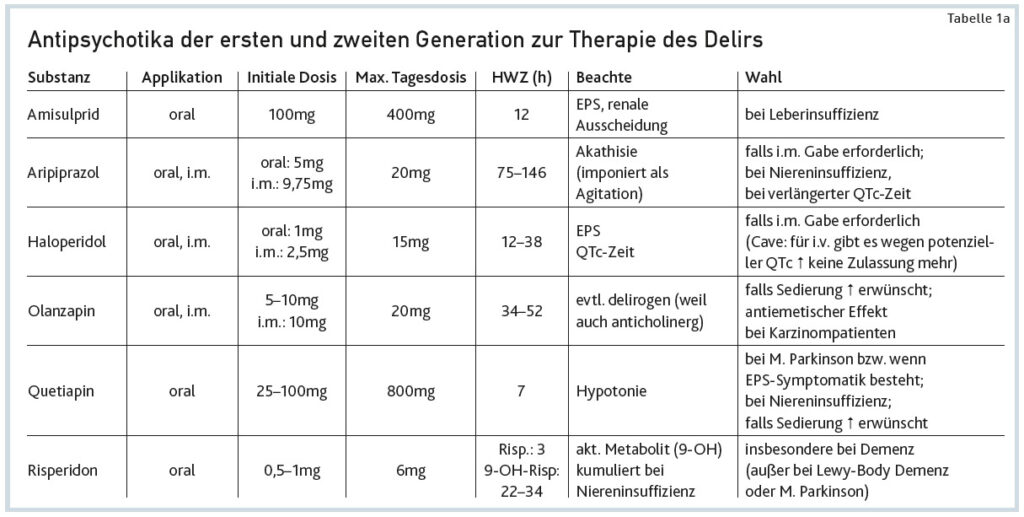
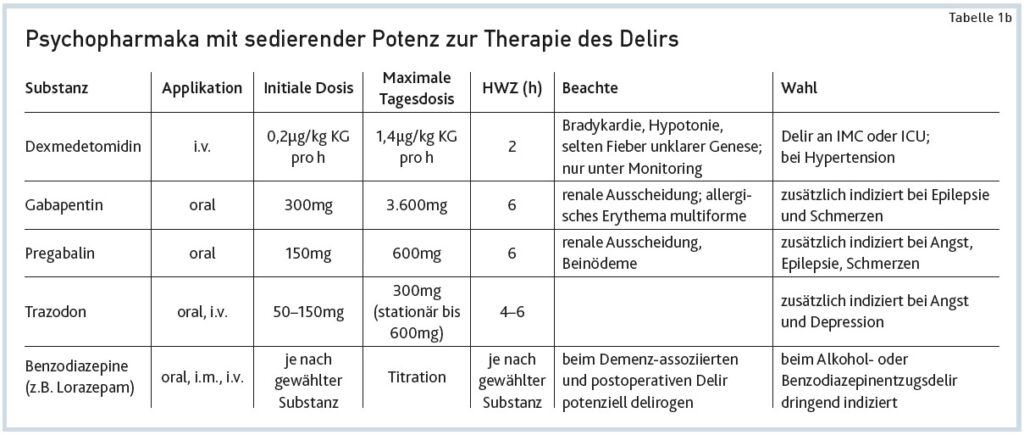
Das Delirium ist ein medizinischer Notfall, in dem die Feststellung und die Therapie der zugrunde liegenden Ursache(n) immer den basalen Schritt der Behandlungskette darstellen (Abbildung 1). Daher sollte sich die Pharmakotherapie in erster Linie auf die Ursache (falls diese bekannt ist) fokussieren. Die Psychopharmakatherapie ist indiziert, um die generellen Symptome des Deliriums (siehe Infobox) auch Ätiologie-übergreifend medikamentös therapieren zu können bzw. um die Dauer und Intensität der Verwirrung zu minimieren (Abbildung 1, Tabellen 1a und 1b). Bei gefährdender Agitation oder produktiv psychotischer Symptomatik ist Psychopharmakatherapie akut erforderlich, bei rascher und deutlicher Entwicklung einer quantitativen Bewusstseinstörung (Somnolenz-SoporKoma) ist hingegen Zurückhaltung geboten.
Man sollte auch an seltene Ursachen des Delirs wie die Autoimmun-Enzephalitis (z.B. Anti-NMDA-Rezeptor Enzephalitis) oder einen nicht konvulsiven Status epilepticus denken, da diese besonderer Diagnostik und vital indizierter Therapie bedürfen. Antipsychotika, deren Wirkmechanismus einen Dopamin-Rezeptor-Antagonismus beinhaltet, sind sowohl für die akute Therapie des Delirs als auch zur Prävention die klinisch relevanteste Substanzgruppe, in Übereinstimmung mit der Annahme, dass ein Dopaminüberschuss an der Pathogenese des Delirs beteiligt ist (Maldonado, 2017). Andere mögliche pathogenetische Faktoren finden bis dato keinen Niederschlag in psychopharmakologischen Therapiestandards zum Delir. Delirante Patienten sind wegen ihrer Verwirrtheit (mit eingeschränkter Einsichtsund Urteilsfähigkeit) und wegen der vitalen Bedrohung aus medizinethischen Gründen kaum in prospektive wissenschaftliche Projekte einzuschließen; so gibt es zum Beispiel bis heute keine publizierte Studie, welche mittels Dopamintransporterszintigraphie (DAT-SPECT, klinisch etabliert zur Parkinson-Diagnostik) die zugrunde liegenden Mechanismen des Delirs erforscht.
Der Einsatz von Antipsychotika beim Delir wird in der Regel mit niedrigeren Dosen als bei schizophrenen Erkrankungen empfohlen. Nach Finden der Zieldosis sollte die Therapie nach Symptomfreiheit noch sieben bis zehn Tage fortgeführt werden. Nicht nur das hypermotorische Delir bedarf dieser antipsychotischen Therapie, auch das hypomotorische Delir, welches oftmals schwerer zu diagnostizieren ist, soll – neben der Behandlung der auslösenden organischen Grunderkrankung – adäquat antipsychotisch behandelt werden. Als diagnostisches Instrument etablierte sich die CAM (Confusion Assessment Method) zur standardisierten Bewertung und Dokumentation des Delirs, geeignet sowohl für die hyperals auch die hypomotorische Form. Abbildung 2 zeigt die CAM-Kurzform, welche im klinischen Routinealltag unkompliziert eingesetzt werden kann. Um die Diagnose Delir stellen zu können, müssen die Items „akuter Beginn und fluktuierender Verlauf “ und „Aufmerksamkeitsstörung“ obligat erfüllt sein, zusätzlich mindestens eines der beiden Items „formale Denkstörung“ und „veränderte Bewusstseinslage“.
Die speziell für Intensivstationen entwickelte Version CAMICU (Confusion Assessment Method for the Intensiv Care Unit) beinhaltet Tests, deren Beantwortung vom Patienten kein Sprechen erfordert ; daher ist sie auch für noch Intubierte geeignet. An Intensivstationen (CAM-ICU) wird die veränderte Bewusstseinslage (Kriterium 4) durch die Richmond Agitation Scale (RASS) mit Scores von minus 5 bis minus 1 (=nicht weckbar bis schläfrig), null (=aufmerksam und ruhig) sowie 1 bis 4 (=unruhig bis agitiert, in extremis aggressiv) beschrieben. Dem digital affinen Mediziner stehen für für eine CAM-ICU-Anwendung bereits Smartphone-Apps zur Verfügung. Wichtige nicht medikamentöse Interventionen beinhalten Hilfestellungen bezüglich kognitiver Einschränkungen, Schlafdeprivation, Immobilität, visueller und auditiver Funktionseinschränkungen sowie Dehydratation (Abbildung 1): Orientierung unterstützen, Schlafprotokolle und rhythmisierende Maßnahmen, Gehhilfen, Hörund Sehhilfen, ausreichend Flüssigkeit (Inouye et al., 1999). Vor einem geplanten operativen Eingriff gehören die Optimierung der internistischen Therapie („interne Freigabe“) und die Präanästhesie und die Vorbehandlung von Substanzabhängigkeiten zum vorbeugenden Standard.

1.1. Medikamentöse Therapie des akuten Delirs
1.1.1. Antipsychotika. Aufgrund des verbesserten Nebenwirkungsprofils kommen heute vermehrt Antipsychotika der zweiten Generation, wie Aripiprazol, Amisulprid, Olanzapin, Quetiapin und Risperidon zur Behandlung von Delirien zum Einsatz; dies wird durch positive randomisierte, kontrollierte klinische Studien (Kishi et al., 2016: Metaanalyse zu Second Generation Antipsychotika (SGA) im Vergleich zu Haloperidol) unterstützt. Eine alphabetische Auflistung, inkl. Dosisangaben, findet sich in der Tabelle 1a zur Antipsychotika-Therapie des Delirs. Risperidon 1–4mg/Tag bietet in der Fachliteratur bessere oder gleichwertige Effizienz im Vergleich zu anderen Antipsychotika oder zum schlechter verträglichen Haloperidol (extrapyramidal motorische Symptome, EPMS bzw. Parkinsonoid). Innerhalb der SGA ist Risperidon relativ wenig sedierend und eine therapeutische Option sowohl beim hyperals auch beim hypomotorischem Delirium. Risperidon in einer Dosisempfehlung von 1–4mg/Tag hat eine Zulassung zur Behandlung von Aggression bei Patienten mit Demenz.
Aggression bei Demenz kommt als Verhaltensstörung oder im Zuge deliranter Entgleisungen vor, aber eine explizite Zulassung zur Behandlung der Diagnose Delir gibt es für Risperidon nicht. Haloperidol hat mit Dosierungsrichtlinien von 1–10mg pro Tag eine Zulassung (siehe Fachinformation) zur Behandlung des akuten Delirs. Andere Antipsychotika stehen in der Behandlung des Delirs außerhalb des durch die Arzneimittelbehörden zugelassenen Gebrauchs („off label“). Lonergan et al. (2007) publizierten in einer Cochrane-Übersichtsarbeit, dass es derzeit keine Evidenz gäbe, dass low-dose Haloperidol (<3mg/Tag), verglichen mit SGA wie Olanzapin und Risperidon, wirksamer bezüglich des Delir-Managements wäre, jedoch wurde unter Haloperidol häufiger ein Parkinsonoid festgestellt. Quetiapin stellt eine valide Option beim deliranten Patienten dar (Tahir et al., 2010, n=42). Die Substanz hat eine relativ kurze HWZ von etwa sieben Stunden und soll daher zweibis dreimal täglich dosiert werden. Bezüglich Sedierungsgrad und möglicher Hypotonie ist vor allem bei älteren Patienten Vorsicht geboten. Quetiapin ist ein nur schwacher D2-Rezeptor-Antagonist und darf daher sogar bei deliranten Parkinson-Patienten eingesetzt werden.

Dopaminergika wie Levodopa und Amantadin wirken potenziell delirogen. Olanzapin wird gemäß der Fachinformation bei Verhaltensstörungen oder Psychosen im Zusammenhang mit Demenzen nicht empfohlen, weil schwere zerebrovaskuläre Ereignisse in sechsbis zwölfwöchigen Studien gehäuft auftraten. Zum Einsatz beim postoperativem Delir gibt es aber positive Ergebnisse (Lonergan et al., 2007; Kishi et al. 2016), obwohl anticholinerge Begleiteffekte zur Vorsicht mahnen. Olanzapin wirkt andererseits über seine multiplen antagonistischen Wirkungen an dopaminergen, serotonergen (inkl. 5-HAT3) und histaminergen Rezeptoren antiemetisch und wird daher gerne bei Karzinompatienten eingesetzt, auch wenn sie bereits kognitiv eingeschränkt oder delirant sind. Aripiprazol ist in der antipsychotischen Behandlung von Delirien eine Alternative (Boettger und Breitbart, 2011, verwendeten im Mittel 18mg), die im Unterschied zu Haloperidol, Risperidon oder Quetiapin noch wenig angewendet wird. Bei deliranten Patienten mit grenzwertigen oder verlängerten QTc-Zeiten stellt Aripiprazol eine wesentliche Option dar, da es nachweislich die QTc-Zeit im Vergleich zu anderen Antipsychotika kaum bis gar nicht beeinflussen dürfte (Marder et al., 2003).
Auch bei älteren hypomotorischen Patienten, welche zu Somnolenz neigen, und bei übergewichtigen Patientinnen ist Aripiprazol eine gute Option, weil die anthistaminerge Rezeptoraffinität, die sedierend und appetitanregend wirkt, nur sehr gering ist. Die Nebenwirkung einer Akathisie kann unter Aripiprazol aber zum klinischen Bild der erhöhten Agitation führen. Ziprasidon zeichnet sich auch durch das geringe Maß an metabolischen Nebenwirkungen aus, aber das Risiko einer QTc-Verlängerung und die große Bandbreite der antipsychotischen Dosierung tragen wohl dazu bei, dass das Präparat weder in der Studienlandschaft noch in der üblichen Off-label-Behandlung des Delirs besondere Berücksichtigung findet. Amisulprid und Paliperidon (9-OH-Risperidon, aktiver Metabolit des Risperidon) stellen die Mittel der Wahl bei deliranten Patienten mit schwerer Leberinsuffizienz dar, da sie renal ausgeschieden werden; die Fachinformationen zu beiden Substanzen schreiben keine Dosisanpassung bei Leberinsuffizienz vor.
Amisulprid sollte zur antipsychotischen Behandlung des Delirs mit mindestens 100mg pro Tag dosiert werden (Lee et al., 2007), weil niedrige Dosen über reine Aktivierung präsynaptischer Autorezeptoren zu verstärkter Dopaminausschüttung führen können. Amisulprid ist eher stimmungsaufhellend und aktivierend als dämpfend und demnach bei stillen, hypomotorischen Delirien zu erwägen, obwohl es zu dieser Differenzierung im Allgemeinen leider keine spezifischen psychopharmakologischen Daten gibt. Quetiapin und Aripiprazol werden rein hepatisch eliminiert und sind somit für Patienten mit Niereninsuffizienz geeignete Pharmaka; die Fachinformationen zu beiden Substanzen schreiben keine Dosisanpassung bei Niereninsuffizienz vor.
1.1.2. Antikonvulsiva. Pregabalin (Tagesdosen von 150mg vor dem Eingriff und bis fünf Tage post OP) konnte die Beatmungsdauer, Opioid-Dosen und Delirien (erfasst mittels CAM-ICU-Scores) bei Älteren nach Herzoperationen reduzieren (Pesonen et al., 2011). Durch Drosselung des Kalziumeinstroms bzw. Stabilisierung der Zellmembran reduziert Pregabalin die Glutamin/ Glutamat und auch die Noradrenalin-Freisetzung in Neuronen. Die Substanz kann aus klinischer Sicht beim Delir jedenfalls zur Entängstigung und Sedierung beitragen. Ein ähnlicher Wirkmechanismus sowie eine antidelirogene Wirkung wurde für Gabapentin beschrieben (Leung et al., 2006), aber in einer großen, placebokontrollierten Studie (Leung et al., 2017) nicht bestätigt. Beide Substanzen werden fast ausschließlich über die Nieren ausgeschieden. Auch Lamotrigin wäre als „glutamat release inhibitor“ zum Off-label-Einsatz beim Delir erwägenswert, aber die große Bandbreite in der Dosierung und das anfangs vorgeschriebene Einschleichen der Dosis wegen des Risikos zum Steven-Johnson Syndrom stellen die Anwendung in der akuten Situation infrage.
1.1.3. Antidementiva. Cholinesterasehemmer, wie Donezepil (Liptzin et al., 2005; Sampson et al., 2007 – beide Studien in der Hüftchirurgie) und Rivastigmin (Gamberini et al., 2009; van Eijk et al., 2010), wurden wiederholt zur Therapie des Deliriums in randomisierten klinischen Studien geprüft (in der Delir-Prophylaxe auch Placebo-kontrolliert) und mit negativen Ergebnissen publiziert. Daher kann keine Empfehlung für den klinischen Einsatz gegeben werden, obwohl die Idee der Stützung der Kognition durch Antidementiva im Delir sehr plausibel und vieldiskutiert ist. Interessanterweise ist eine Studie zum Einsatz dieser Antidementiva beim Delir bei Demenz (ICD-10: F05.1) ausständig. Der Einsatz des Antidementivums Memantin (5–10mg Tagesdosis), ein NMDA-Rezeptor-Antagonist (bei dem auch der Wirkmechanismus von Pregabalin, Gabapentin oder Ketamin ansetzt), ist beim Delir vielversprechend, aber Ergebnisse wurden noch nicht veröffentlicht.
1.1.4. Kortikosteroide. Delirien werden partiell auch durch neuroinflammatorische Prozesse erklärt, bei welchen proinflammatorische Zytokine eine synaptische Dysfunktion und neuronale Schädigungen hervorrufen (Maldonado, 2017). Diese Entzündungskaskade kann durch operative Eingriffe getriggert und daher durch Kortikosteroide gebessert werden. Eine randomisiert kontrollierte Studie an 93 Patienten mit einer Dosis von 8mg Dexamethason intravenös vor und nach der Operationen zeigte, dass die Dexamethason-Gruppe am ersten postoperativen Tag weniger Delirien im Vergleich zur Placebogruppe (16,3% vs. 38%, p=0,03) und auch eine verkürzte stationäre Aufenthaltsdauer verzeichnete. Diesen Daten widerspricht jedoch eine wesentlich größere Mulitcenter-Studie mit 7.507 Teilnehmern, welche Methylprednisolon versus Placebo während einer Bypass-OP erhielten, wobei dies keinen Effekt bezüglich der Delir-Inzidenz zeigte (Siddiqui et al., 2016).
1.1.5. Melatonin spielt eine Rolle bei der Regulation des zirkadianen Rhythmus bzw. der Schlaf-Wach-Phasen, welche bekanntlich beim Delir gestört sind. Patienten mit einem hyperaktiven Delir zeigen niedrigere Melatonin-Werte im Urin verglichen mit nicht deliranten Patienten. Studien konnten mit 5mg Melatonin abends perioperativ (Sultan et al., 2010) oder mit 0,5mg abends in gerontologischer Indikation (Al-Aama et al., 2011) positive Effekte hinsichtlich der Delirentwicklung zeigen, während de Jonghe et al. (2014) diesen Effekt bei Hüftfrakturen nicht beobachten konnten. Die Datenlage ist also widersprüchlich.
1.2. Möglichkeiten zur Sedierung des agitiert deliranten Patienten
Es ist wichtig zu erwähnen, dass Delirien im klinischen Alltag trotz adäquater pharmakologischer Therapie Zeit brauchen, um abzuklingen. Durchschnittlich dauert das postoperative Delir zwar nur einen bis vier Tage, aber nicht selten besteht die delirante Symptomatik auch über mehrere Wochen hinweg, je nachdem wie gut sich die letztlich multiplen organischen Ursachen behandeln lassen, was bei alten Patienten besonders schwierig ist. Auch findet der Einsatz von Benzodiazepinen (oft mangels Wissen an Alternativen) zu häufig statt. Diese stellen zwar beim stark agitierten Patienten eine Option dar, jedoch auch immer im Wissen, dass Benzodiazepine per se ein delirogenes Potenzial beinhalten.
1.2.1. Antipsychotika zur Sedierung. Umfassende systematische Konsensus-Statements der World Federation of Societies of Biological Psychiatry (WFSBP) (Garriga et al., 2016) und der Österreichischen Gesellschaft für Neuropsychopharmakologie und Biologische Psychiatrie (ÖGPB, Kasper et al., 2013) zur Therapie der Agitation empfehlen neben der verbalen Deeskalation des agitierten Patienten den peroralen Einsatz von Second-Generation-Antipsychotika (SGA); in diesen Konsensus-Statements steht schon einleitend, dass bei psychomotorischer Agitation im ersten Schritt in einer medizinischen Untersuchung auf mögliche somatische Ursachen geachtet werden muss (Abbildung 1), insbesondere wenn der Patient im fortgeschrittenen Alter ist. Bei klinischen Prüfungen innerhalb der Psychiatrie werden zur Einstufung der psychomotorischen Agitation Rating Scales wie die Agitation Severity Scale (ASS, Strout 2014) oder die Positive and Negative Syndrome Scale – Excited Component (PANSS-EC, Kay et al., 1987) verwendet, die im Wesentlichen an schizophrenen Patienten validiert sind.
In dieser Indikation zeigten Olanzapin, Quetiapin und Risperidon im Vergleich zu Haloperidol eine gleichwertige Effektivität gegen Agitation (Kasper et al., 2015), aber in den Haloperidol-Gruppen fanden sich signifikant mehr extrapyramidal motorische Symptome (EPMS). Das deckt sich mit den oben genannten Studienergebnissen zur Antipsychotikatherapie des (hypermotorischen) Delirs. Während bei Schizophrenie und auch bei Manie zur Sedierung die Kombination SGA plus Benzodiazepin (wesentliche Prüfsubstanz: Lorazepam) der Monotherapie mit einer der beiden Substanzgruppen überlegen ist, haben die Benzodiazepine in der Behandlung des Delirs kaum Evidenz und zweifellos Risiken. Oftmals wäre wegen der eingeschränkten Kooperationsfähigkeit bei deliranten Patienten eine akute intravenöse Sedierung vonnöten. Haloperidol i.v. ist wegen des Risikos der QTc-Verlängerung nicht mehr zugelassen, und man sucht nach Alternativen der raschen Applikation. Hier ist an Haloperidol i.m. oder – besser verträglich – auch an Aripiprazol i.m. zu denken. Aripiprazol (9,75mg/1,3ml Injektionslösung) intramuskulär ist zur schnellen Kontrolle von Agitiertheit bei Schizophrenie oder bei manischen Episoden zugelassen und war in kontrollierten Studien in dieser Indikation äquipotent gegenüber 10mg Haloperidol i.m..
In Anbetracht der oben erwähnten positiven Studien zu Aripiprazol-Tabletten beim Delir erscheint der Übergang zur intramuskulären Off-label-Anwendung beim hypermotorischen Delir sinnvoll und verantwortbar. Die kurzfristige Gabe von Olanzapin i.m. (10mg/2,1ml Injektionslösung) kann trotz bekannter anticholinerger Begleiteffekte zur Sedierung beim Delir auch erwogen werden; die Studien zum postoperativen Delir haben immerhin positive Ergebnisse gebracht, auch intramuskulär (Kishi et al., 2016). In der Fachinformation wird Olanzapin bei Demenz nicht empfohlen (siehe oben), des Weiteren wird die Kombination von Olanzapin i.m. und Benzodiazepinen i.v. für unsicher erachtet.
1.2.2. Benzodiazepine werden in der Praxis immer wieder auch beim nicht alkoholentzugsbedingten hypermotorischen Delir eingesetzt und in der Literatur kontrovers diskutiert. Zusammenfassend sind Benzodiazepine bei nicht substanzinduzierten Delirien ohne Evidenz (Lonergan et al., 2009: Cochrane Review). Tatsächlich sind Benzodiapezine potenziell delirogen. Verwirrtheitszustände können aggravieren, weil die Vigilanz bzw. die Aufmerksamkeit getrübt wird; daher sind paradoxe Wirkungen, d.h. Agitation wegen des abnehmenden Realitätsbezuges, möglich. Darüber hinaus stellen erhöhte Sturzgefahr und Aspirationsgefahr oder Übersedierung weitere mögliche Komplikationen dar, weshalb man die Gabe von Benzodiazepinen nur bei mangelnden Alternativen in Erwägung ziehen sollte. Mit Pregabalin (siehe oben) können wohl auch Benzodiazepine eingespart werden.
1.2.3. Trazodon ist auch anxiolytisch und sedierend und steht sowohl zur oralen als auch intravenösen Applikation (50mg Ampullen, bis zu dreimal täglich) zur Verfügung. Eine kürzlich publizierte Arbeit (Wada et al., 2018) zeigte ähnlich wirksame Effekte für Trazodon wie für Quetiapin in der Delirbehandlung.
1.2.4. Dexmedetomidin wurde während der vergangenen zehn Jahren in doppelblinden randomisiert kontrollierten Studien im Zusammenhang mit Beatmung, schweren somatischen Erkrankungen und Delirien untersucht (Pandharipande et al., 2010), sodass die Substanz mittlerweile zur intravenösen Sedierung intensivmedizinisch behandelter Patienten zugelassen ist. Dexmedetomidin ist ein Alpha-2-Agonist. Der Einsatz von Dexmedetomidin in Perfusoren in kontinuierlicher Verabreichung (Dosierung in Mikrogramm pro kg KG laut Tabelle 1b) ist an Allgemeinstationen jedoch kaum möglich, da das Setting ein Monitoring der Vitalparameter erfordert, weil arterielle Hypotonie und Bradykardie als Begleiteffekte auftreten und die Durchflussrate sowohl danach als auch nach der Sedierungstiefe titriert werden muss. Als Alternative zu Dexmedetomidin ist der zurzeit noch kostengünstigere, ältere Alpha-2-Agonist Clonidin zu erwägen, welcher auch in peroraler Applikationsform (zweibis dreimal täglich 0,075 oder 0,15mg) verabreicht werden kann. AVBlock, schwere Bradykardie und Hypotonie sind Kontraindikationen für den Einsatz von Alpha-2-Agonisten.
1.2.5. Opioide. In Hinblick auf die medikamentöse Prävention des Delirs an Intensivstationen wird unten noch auf Opioide eingegangen. An der Psychiatrischen IMC der Universitätsklinik in Wien (UKPP) wird bei schwerer Agitation und Schlaflosigkeit off label Nalbuphin 10 bis 20 mg s.c. zur Sedierung mit einer Wirklatenz von 15 Minuten und einer Wirkdauer von drei bis sechs Stunden erfolgreich angewendet, in der Regel ohne Atemdeprivation.
2. Medikamentöse Prävention des postoperativen Delirs
Medikamentöse prophylaktische Maßnahmen für Patienten mit hohem Delir-Risiko (hohes Alter; Intensive Care Unit, ICU) sollten die Inzidenz, die Länge und den Schweregrad der deliranten Episoden reduzieren und dadurch die Aufenthaltsdauer im stationären Bereich verkürzen. Um klare klinische Empfehlungen für die medikamentöse Prävention des Delirs durch Antipsychotika abgeben zu können, ist die Datenlage immer noch zu spärlich (NICE, 2010), obwohl es positive Befunde in randomisierten doppelblinden Placebo-kontrollierten Studien gibt (Göttel und Steiner, 2013), beispielsweise zur präoperativen Gabe von Haloperidol 1,5mg, das den Schweregrad und die Dauer von Delirien reduzierte (Kalisvaart et al., 2005, n=430), oder zu Olanzapin 5mg, welches die Inzidenz reduzierte (Larsen et al., 2010, n=495); beide wurden kurzzeitig perioperativ p.o. in der Hüftchirurgie gegeben.
Risperidon 1mg in der Herzchirurgie postoperativ unmittelbar beim Aufwachen reduzierte die Delirinzidenz im randomisierten doppelblinden Placebokontrollierten Design signifikant (Prakanrattana et al., 2007, n=126). Ebenso haben die intraund postoperativ verwendeten Anästhetika und Sedativa einen Einfluss auf die Entwicklung eines Delirs. Die Tiefe der Sedierung dürfte eine bedeutende Rolle bei der Delirentwicklung spielen, weshalb Studien nahelegen, so wenig tief wie nur möglich zu sedieren. Die Literatur beschreibt des Weiteren den Terminus des ABCDE-Bundle (Awakening and Breathing Coordination, Delirium Monitoring and Early Mobility Bundle), welches die Prävalenz von Delirien senken sollte (Girard et al., 2008). Es wird ein Zusammenhang zwischen Sedierungsgrad und Delir gesehen; bei Midazolam kommt es zu einer prolongierten Aufwachphase, welche einen negativen Prädiktor für die Entwicklung eines Deliriums darstellt.
Propofol führte im Vergleich zu Benzodiazepinen zu einer verkürzten Aufenthaltsdauer auf Intensivstationen (Ho und Ng, 2008). Bei genauerer Durchsicht der Literatur ist die Datenlage für Propofol jedoch noch widersprüchlich. Peri und postoperativ bewährte sich der Einsatz von Opioiden gegenüber dem schlechteren Outcome mit Midazolam. Radtke et al. (2010) zeigten diesbezüglich eine verminderte postoperative Delirinzidenz bei Remifentanyl i.v. (HWZ nur drei Minuten) verglichen mit Fentanyl i.v. (HWZ 47 Minuten). Aus der vergleichenden Studie mit intravenöser Applikationsform in Allgemeinanästhesie lässt sich aber nicht schließen, dass eine analgetische Behandlung mit transdermalem Fentanyl delirogen wäre. Bezüglich des Einsatzes von Opioiden als postoperative Schmerztherapie soll auf die Substanz Phetidin (ältestes vollsynthetisches Opioid, Atropin-Abkömmling) verzichtet werden.
Die prolongierte mechanische Beatmung ist ein Risikofaktor für Delirien. Bei der Beatmung unter Dexmedetomidin i.v. Perfusor (siehe oben) konnte die Zeitspanne am Respirator, verglichen mit Midazolam und Propofol, reduziert werden, die Patienten konnten eher Schmerzen äußern, es traten jedoch auch häufiger kardiovaskuläre Nebenwirkungen (Bradykardie, Hypotonie) auf (Venn et al., 1999, Maldonado et al., 2009). Exzitatorische Aminosäuren, wie die Transmitter Glutaminsäure und Asparaginsäure (bzw. deren ionisierte Form Glutamat und Aspartat), fungieren als Agonisten an den ionotropen NMDA(N-Methyl-D-Aspartate)-Rezeptoren, und gerade im chirurgischen Setting bzw. bei Entzündungsreaktionen kann über die NMDA-Rezeptorvermittelte Öffnung von Kationen-Kanälen eine exzitatorische Apoptose getriggert werden.
Ketamin, ein Antagonist am NMDA-Rezeptor, hat somit das wissenschaftlich begründete Potenzial gegen eine solche Zellschädigung im ZNS (die postsynaptischen NMDA-Rezeptoren finden sich insbesondere im Hippocampus und im Großhirn) zu schützen. Daher erscheint Ketamin als plausibles präventives Agens beim intensivmedizinischen Management des postoperativen Delirs. Es konnte gezeigt werden, dass die einmalige Verabreichung von Ketamin oder S-Ketamin 0,5mg/kg Körpergewicht zur Einleitung der Anästhesie bei Herzoperationen zu einer verminderten Entzündungsreaktion und einer sehr geringen Delirinzidenz von drei Prozent führte (Hudetz et al., 2009). Ketamin hemmt auch HCN1-Kanäle (hyperpolarization activated cyclic nucleotidegated channel), die im ZNS wichtig für die Regulation des Bewusstseinsgrades („Schrittmacherkanäle“) sind. Daher scheint auch diese Wirkung in Bezug auf das Delir relevant zu sein.
Eine rezent erschienene „Lancet“-Publikation einer randomisierten klinischen Multicenter-Studie mit 672 Patienten konnte jedoch keine präventiven Effekte von nach der Narkoseeinleitung applizierten Ketamin 0,5–1mg/ kg KG Einzeldosen bezüglich postoperativem Delir aufzeigen (Avidan et al., 2017). Zur konsekutiven Anwendung als Dauerinfusion zur Analgesie bei künstlicher Beatmung gibt es in der Fachinformation eine Zulassung, aber noch keine Daten bezüglich des Einflusses auf Delirien. Magnesium ist ein kompetitiver Blocker am ionotropen NMDA-Rezeptor, und es gibt Studien, die zeigen, dass kontinuierlich im Perfusor verabreichte intravenöse Magnesiumsulfat-Dosen (woraus Magnesium-Plasmaspiegel um 2mmol/l resultieren) sedieren können (NaderiHeiden et al., 2005).
Bezüglich der Einnahme von Beta-Blockern vor einer Operation und dem Auftreten eines postoperativen Delirs zeigt sich die Datenlage widersprüchlich. Während Katznelson et al. (2009) im Rahmen von gefäßchirurgischen Eingriffen eine erhöhte Delirinzidenz unter BetaBlocker-Therapie zeigten, gab es in einer rezenten herzchirurgischen Kohorte von O´Neal et al. (2017) keinen signifikanten Hinweis auf einen derartigen negativen Effekt. Propranolol, ein nicht selektiver beta-adrenerger Antagonist, welcher die Blut-Hirn-Schranke sehr leicht passiert, kann eine signifikante Reduktion der Dosis von Sedativa und Analgetika herbeiführen und ist daher möglicherweise eine sinnvolle Add-on-Therapie beim Delirium. Bisher gibt es jedoch nur Fallbeobachtungen und noch keine kontrollierten Studien (Shiotshuka et al., 2017).
Auch Statine finden vermehrt Einzug in die Delir-Forschung, da diese aufgrund ihrer pleiotropen Effekte auf molekulare Stoffwechselwege von Entzündungsreaktionen und endothelialen Funktionen positiv wirken könnten. Mather et al. (2017) konnten in ihrer Arbeit erheben, dass der Einsatz von Statinen während der intensivmedizinischen Behandlung das Risiko eines Delirs senken konnte. Atorvastatin, Pravastatin und Simvastatin konnten diese Effekte vorweisen. Weitere randomisiert kontrollierte Studien wären hierfür noch notwendig. In einigen Studien bedingt das Design mit der perioperativen Gabe der Pharmaka, womöglich über die Beatmung hinaus, dass eine Vermengung von präventiven und akuten antidelirogenen Effekten gegeben ist.
3. Behandlung des Delirium tremens im Alkoholentzugssyndrom
Benzodiazepine in hohen Dosen, wie Diazepam (oral 10–20mg bis zu viermal täglich, i.v. bis 10mg/Stunde) oder Lorazepam (oral 2,5–5mg bis zu viermal täglich, i.v. 2–4mg/Stunde), stellen die Therapie der Wahl bei substanzgebundenen Entzugsdelirien dar (Kasper et al., 2013). Die extrem hohen Dosisempfehlungen sind beim alkoholischen Delirium tremens publiziert (Mayo-Smith et al., 2004; Soyka et al., 2008: WFSBP Guidelines). Die Kumulation der Benzodiazepine stellt ein Risiko dar, weshalb Lorazepam als Mittel der Wahl vorgeschlagen wird, weil Lorazepam eine HWZ von <20 Stunden hat, keine aktiven Metaboliten aufweist und in seiner intravenösen Darreichungsform beim Delirium tremens explizit zugelassen ist. Falls eine perorale BenzodiazepinTherapie für ausreichend erachtet wird, ist Oxazepam (hat keinen aktiven Metaboliten) in Tagesdosen bis etwa 400mg eine Alternative.
Benzodiazepine wirken entspannend und antikonvulsiv und bessern die profusen vegetativen Begleiterscheinungen (Zittern, Schwitzen, Tachykardie) (Amato et al., 2010). Des Weiteren ist auf eine ausreichende Flüssigkeitszu fuhr und einen ausgeglichenen Elektrolytund Vitaminhaushalt mit regelmäßigen Blutkontrollen zu achten; bei Verdacht auf Wernicke-Enzephalopathie müssen Vitamin B1 (=Thiamin) Infusionen hochdosiert (100–500mg i.v./Tag) täglich über drei Wochen erfolgen. In Deutschland und der Schweiz wird auch Clomethiazol (ein Thiazolderivat chemisch mit dem Vit B1/Thiamin verwandt, kurze HWZ) in Tagesdosierungen von vierbis achtmal zwei Kapseln à 192mg erfolgreich zur Behandlung des Entzugsdelirs bzw. zur Sedierung eingesetzt.
Die Alpha-2-Agonisten Clonidin und Dexmedetomidin haben sedative Eigenschaften und sind besonders bei arterieller Hypertonie und Tachykardie und Benzodiazepinrefraktärer Agitation im Alkoholentzugsdelir sinnvoll. Haloperidol oder atypische Antipsychotika sind beim Entzugsdelir nicht angeraten, da es keine Evidenz für Wirkung gibt, aber bekanntermaßen Nebenwirkungen bestehen (EPS, arrhythmogen, epileptogen). Carbamazepin, Valproinsäure und Topiramat erbrachten Wirknachweise bei der Alkoholentzugstherapie, jedoch nicht beim Alkoholentzugsdelir. Nach klinischem Ermessen besteht auch für Pregabalin eine off label Indikation.
4. Zusammenfassende Empfehlungen
Die gebotenen Daten zur Pharmakotherapie des Delirs basieren vor allem auf Erkenntnissen zum häufigen postoperativen Delir bei älteren Menschen an Intensivstationen oder in Fächern mit chirurgischen Interventionen. Selbstverständlich sind gleichzeitig auch die Psychiatrie und die Geriatrie besonders gefordert. Ältere Menschen mit inzipienten oder manifesten Demenzen sind vulnerabel und besonders häufig von Delirien in Krankenhäusern betroffen. Man kann annehmen, dass die vorgestellten psychopharmakologischen Empfehlungen im Wesentlichen auch für die Behandlung des Delirs bei Demenz gelten. Unter den Antipsychotika sind primär Risperidon und Quetiapin per oral zu empfehlen. Wenn eine parenterale Applikation kurzfristig indiziert ist, ist die intramuskuläre Injektion von Aripiprazol off label eine therapeutische Option.
Pregabalin wird aufgrund seiner Pharmakodynamik in der klinischen Routine bereits fallweise erfolgreich beim Delir eingesetzt, aber dies schlägt sich erstaunlicherweise noch kaum in Publikationen nieder (Pesonen et al., 2011). An Intensivstationen und Intermediate-Care-Stationen (auch an der Universitätsklinik für Psychiatrie und Psychotherapie der Medizinischen Universität Wien) ist der Einsatz von Dexmedetomidin in Perfusoren zur Sedierung bei deliranten Zustandsbildern bereits gut etabliert ; gleichzeitige Pulsoxymetrie und (nicht invasive) Blutdruckmessungen sind dafür Bedingungen. Als Alternative bietet sich bei normotonen oder gar hypertonen Patienten die perorale Verabreichung von Clonidin-Tabletten zur Beruhigung an. Bei Demenz ist zusätzlich zu all dem ein Antidementivum indiziert, wobei die Cholinesterasehemmer in der Behandlung des postoperativen Delirs leider keinen Stellenwert erlangt haben, aber der Einsatz von Memantin (10mg Tagesdosis) erwogen werden sollte.
Literatur bei den Verfassern
Von Dr. Michaela-Elena Friedrich MSc, O.Univ.-Prof. Dr.hc.mult. Dr. Siegfried Kasper und Univ.-Prof. Dr. Richard Frey
Lecture Board: Prim. Dr. Christa Radoš, Prof. Dr. Michael Rainer
Ärztlicher Fortbildungsanbieter: Klinische Abteilung für Allgemeine Psychiatrie, Universitätsklinik für Psychiatrie und Psychotherapie, Wien